(原文链接https://mp.weixin.qq.com/s/7KPcGnMAOoBWZg52beRNrA)
1.什么是脑卒中?
脑卒中(Stroke),又称中风,作为一种急性脑血管疾病,是由于脑部血管突然破裂或因血管阻塞导致血液不能流入大脑而引起脑组织损伤,包括缺血性和出血性卒中。脑卒中是全球第二大死因,在中国是主要死因。中国每年估计有1100万脑卒中患者,每年新发240万脑卒中病例。
脑卒中发病示意图
2.运动功能康复的必要性和临床评估现状
无论缺血性脑卒中还是出血性脑卒中,只要累及运动皮层,运动前区,运动传导通路或者与运动相关的小脑通路都会引起运动功能障碍;约80%的脑卒中患者有运动功能障碍,它会严重影响患者的日常生活,妨碍其重返社会,所以促进脑卒中患者运动功能康复是康复工作者的工作和研究重点
运动功能的准确评估是对于患者的康复非常重要,包括精准制定个性化的康复方案,准确掌握康复治疗效果,以及深入了解运动康复方案背后的机制。而目前临床上最常用的运动功能评估还是临床量表评估为主,常用的量表有:
上肢功能评估量表:
Action Research Arm Test (ARAT) (Lyle 1981) 、Box and Block Test (Desrosiers 1994; Mathiowetz 1985)、Wolf Motor Function Test (WMFT) (Wolf 2001)
手功能评估:
Stroke Impact Scale (Duncan 1999)、Nine‐Hole Peg Test (Kellor 1971)、ABILHAND (Gustafsson 2004)
运动障碍量表:
Fugl‐Meyer Assessment of Sensorimotor Recovery after Stroke (Fugl‐Meyer 1975)、Motor Club Assessment (Ashburn 1982)、Motricity Index (Demeurisse 1980)
肌张力量表:
Ashworth Scale (Ashworth 1964)、Modified Ashworth Scale (Bohannon 1987)
步行能力评估量表:
The Ten Meter Walk Test 、The Six-Minute Walk Test.
尽管临床量表评估已经被广泛接受和应用,也有标准化和验证,但是它还是存在一些不足,例如比较主观,由于是序数量表效率低下,存在天花板效应和地板效应,评估时间较长不利于日常规律管理和追踪患者功能变化,多数临床量表评估无法区分特定肢体功能和代偿功能等。
3.运动功能康复定量化评估技术
(1)肢体及运动功能评估
三维运动分析技术可以客观量化评估肢体功能,联合临床量表评估可以准确区分肢体功能恢复和代偿运动,更能准2确判断预后。
运动追踪技术可以通过各种追踪、存储的传感技术定量的记录运动情况;基于摄像头的运动捕捉技术,像 Vicon (Vicon Motion Systems, Oxford, UK) and Optitrak (Northern Digital Inc, Ontario, CA),需要在体表的一些关键部位放置标记物或者传感器来重建人体骨骼模型,可以高精度、高采样率追踪运动,由于操作较复杂且分析数据费时,一般多在实验室应用。还有一些直接测量加速度、旋转变化和磁定向的运动分析技术,由于使用惯性传感器测量,存在惯性漂移、噪声干扰和校准错误及需要经常充电等不足,而导致测量精度下降。

体表放置marker的运动捕捉
(2)肌肉功能评估
a.肌电(Electromyography, EMG)检测技术
肌电信号(EMG)是在运动神经元激励下由大量运动单位(Motor Unit)兴奋发放的运动单位动作电位序列(Motor Unit Action Potential Train,MUAPT)沿肌纤维传播在检测电极处的时间、空间叠加合成的结果,是与肌肉收缩紧密相关的神经肌肉活动电特性的表现。
最早在 1950 年代,像Thomas Twitchell 这样的临床医生使用 EMG 来监测肌肉活动,表面肌电技术(sEMG)通过在皮肤表面采集肌肉电信号,提供了非侵入性观察肌肉活动的方法,通过监测肌肉活动及观察最终的运动,可以了解神经运动通路的完整性[12]。表面肌电sEMG 最早用于肌肉生理学研究,在随后的几十年中被用作微创的针 EMG 的替代方法,用于评估从手术决策到运动增强的广泛场景[13]。
现有研究表明 sEMG 有助于预测长期恢复、了解肌肉活动特征和肢体间协调、量化步态中的动态运动控制参数、提供生物反馈以及跟踪成人和儿童对康复治疗或手术干预后的反应。但是目前sEMG并未在临床上广泛应用,其中一个可能因素是sEMG的正确解释仍有争议。
另外,在动态条件下许多不可控因素会影响记录sEMG,此时难以直接对比分析受试者之间或肌肉收缩之间的结果,降低了从 sEMG 信号中提取信息并应用于临床的潜力[14]。另外,大多数的传统sEMG都是单一通道(由两个差分电极和信号地组成),会因接触检测面积较大而导致MUAP叠加较多,所以检测到的信号空间分辨率较低,无法较清楚的看到具体MUAP序列发放情况。
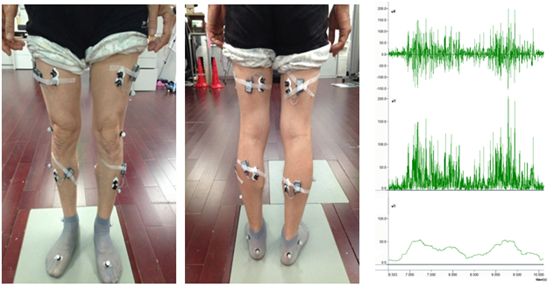
股四头肌表面肌电信号实例, 步行中下肢肌肉sEMG监测
相对于传统的表面肌电技术,高密度阵列表面肌电(High-density sEMG),由许多具有相对较小皮肤-电极接触面(直径可小于2mm)的电极接触点,以较小的间距(可以在5mm以内)排成阵列形式。通过MUAP分解技术(decomposition algorithm),HDEMG还可描述自发性运动单位动作电位放电(Spontaneous MUAP spikes)以及运动单位动作电位发放率(MUAP discharge rate)等信息,是传统的表面肌电无法比拟的。HDEMG肌电分解方法可以用于检验运动单位募集控制紊乱和发放模式可能对肌无力做出的贡献,因为运动单位的重组可能与患者运动功能障碍程度有关。
HDEMG除了能获取肌肉活动的时域信息外,还可获取肌电信号的空间信息。利用高密度表面肌电采集技术可以提供肌电信号的整体分布,可检测神经支配区位置(Innervation zone, IZ) 及测量计算肌纤维传导速度(Muscle fiber conduction velocity, MFCV)等参数,并进行不同肌肉肌腱单元发力特性的估计等。sEMG 信号显着依赖于各种生物力学因素,当大多数影响 sEMG 信号的因素是已知的、可控的并且明确时,可以从肌电振幅中得出可靠的结论。例如涉及等长收缩的应用中就是这种情况,sEMG 信号幅度依赖于收缩类型和关节位置,在等长收缩中,肌肉的力臂和关节的旋转中心保持不变。但是在临床实践中,非等长收缩占主导地位,未来需要新的和创新的 sEMG 采集、处理和信息提取策略使其更适用于临床,并满足医生和治疗师的需求。

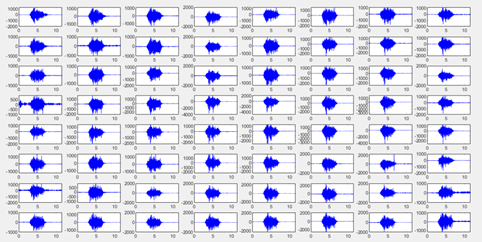
高密度表面肌电(HDEMG)记录和信号
b.肌骨超声
近40年来,越来越多的康复工作者采用超声成像来评估肌肉形态与结构。超声成像通过皮肤表面的探头发出超声波,声波穿透组织,然后通过反射回的声波信息来成像[16]。超声检测提供了一种以非侵入性方式评估肌肉形态学和形态学特征的简单且廉价的方法。超声成像应用医学成像技术对肌肉肌腱参数测量和评估可以配合患者不同姿势和检查条件,包括在其他生物力学设备(例如等速肌力测试系统)下测量,有助于深入探讨肌肉发力情况下以及不同关节角度下肌肉肌腱形态变化。例如应用超声这一重复性好、临床应用简便和无创性的检查,可以揭示脑卒中后患者肘关节肌肉肌腱参数的改变情况,例如肌纤维长度缩小,并且这些参数和关节所处位置有关和发力情况也直接相关。而且研究表明肌骨超声检查在检查者内部及检查者间检查结果均有良好的可靠性。
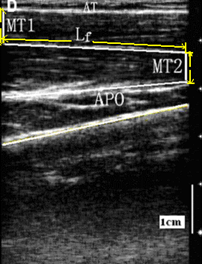
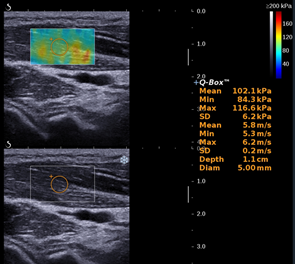
左图:超声显像肌肉结构参数;右图:一位脑卒中患者偏瘫侧和非偏瘫侧桡侧腕屈肌剪切波成像
如何快速量化的评估肌肉的硬度变化在临床上是一大难题,超声剪切波弹性成像技术(Supersonic shear wave elastography, SSWE) 有望解决这一难题。SSWE是近几年新出现的成像方法,利用一个探头发出脉冲,可以使组织内部产生瞬时剪切波,然后收集组织反射的射频数据,通过计算软件对返回的数据进行分析,评估在压迫过程中组织产生的细微的位移差别,从而得到剪切波在组织内的速度差别进行成像超声成像。在传统弹性成像的基础上,剪切波弹性成像允许使用磁共振成像或超声成像测量 SW 速度,这与刚度有关,特别是剪切模量:
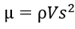
其中,μ 是弹性剪切模量,ρ 是肌肉质量密度(ρ ≈ 1000 kg m-3),Vs 是 SW 速度。组织越硬,SW 移动的速度就越快[18] 超声剪切波技术给无创评估肌肉内部微观结构的弹性提供可能。
c.肌肉电阻抗
肌肉电阻抗技术(EIM)由生物电阻抗分析技术(BIA)演变而来,生物电阻抗技术作为一种无创性的营养评估方法被广泛应用。传统的 BIA 技术基于适当的方程估计全身体积、质量、无脂肪质量或其他分隔的身体成分,此类测量需要针对特定人群的模型,并且通常会受到多种因素的影响,包括水合作用、脂肪含量和几何边界条件;与BIA不同的是,EIM技术设置时间短,重复性好,在脑卒中肌肉状况评估中有良好的前景。EIM 应用弱交流电来评估肌肉电阻和电容特性,肌肉电阻 (R) 定义为骨骼肌对通过细胞外液和细胞内液的电流的固有电阻率。肌电抗 (X) 表示由细胞膜、组织界面和非离子物质引起的传导延迟。电阻(R)和电抗(X)都与肌肉长度成正比,与肌肉的横截面积成反比,受肌肉质量、形状和组织质量的影响。为了减少肌肉解剖对阻抗分析的影响,使用相位角来描述电阻和电抗之间的关系(θ = arctan (X/R)),相位角可以评估细胞膜特性。肌肉的另一个重要特征是其各向异性,表现为肌肉阻抗的方向依赖性。肌肉各向异性表示纤维排列的柱状有序程度。
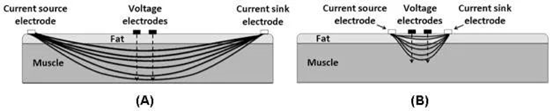
肌肉电阻抗测量示意图
d.Myoton 无创肌肉检测技术
Myoton 是一种手持设备,可提供客观的肌肉的三种机械特性的测量:张力、刚度和弹性。 振荡频率 (Hz) 表示肌肉在静息状态下的张力(即内在张力)。肌肉自然振荡的对数衰减表示肌肉的弹性,如它在收缩后恢复形状的能力。动态刚度 (N/m) 表征肌肉对收缩的抵抗力。通过肌测量法计算肌肉刚度会受到覆盖肌肉的皮肤的设备的小扰动。加速度计测量肌肉的变形特性,并使用肌肉反冲特性所表现出的阻尼自然振荡来计算刚度。
(3)脑及中枢神经系统评估
a.功能磁共振检测(fMRI)
fMRI是一种可以检测大脑活动变化的无创性成像技术,它依靠氧合血红蛋白和脱氧血红蛋白的磁性来检测由神经元活动引起的局部血流变化(血氧水平依赖性 [BOLD] 反应);当神经元活跃时,流向该区域的血流量会增加,以满足通过神经血管耦合增加的氧气需求。这使得我们可以对任务或刺激的反应进行定位和量化,使用 BOLD 反应作为神经元活动的代表。由于功能性 MRI (fMRI) 不使用电离辐射、化学示踪剂或需要侵入性手术/植入物,因此它是对脑卒中进行临床研究的理想方法,特别是研究运动功能恢复的中枢机制方面。
任务诱导 fMRI 研究需要功能受损患者的积极参与,此外还依赖于可能不会激活所有感兴趣组织的特定任务设计。而静息态 fMRI无需患者配合,可以同时探索整个大脑中所有功能网络,它与弥散 MRI 作为主要白质束“结构连通性”的补充测量相结合,在没有任务的情况下探测整个大脑功能的能力可能可以更大程度地解释中风后的广泛行为变化[24]。最近使用静息状态 (RS) fMRI 的研究已经确定了与恢复相关的功能连接的变化。在中风后的急性阶段,即使在病变区域以外的区域,半球间的连通性也大大降低。这最初被认为是由于未受损的半球影响了受损的半球,因为未受损的区域补偿了丢失的组织,连接性随着恢复变得更加平衡。
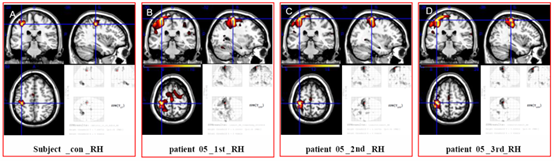
b.功能近红外光谱检测(fNIRS)
fNIRS 近年来已成为神经科学领域的一项非常有吸引力的技术,40 年前,Jöbsis 首次描述了它,其具有便携性、耐受性、非侵入性、成本效益和长期实时监测能力等特点。
它的原理在于波长在650—925nm的光波被氧合血红蛋白和脱氧血红蛋白吸收量远远大于周围组织,通过测量不同血红蛋白种类的光吸收变化,可以使用 fNIRS 计算脑血流量的时间变化,通过检测不同吸光分子相对浓度的变化,fNIRS 可以分析大脑中的能量代谢。
例如,fNIRS 可以以类似于 fMRI 的方式测量氧合和脱氧血红蛋白的变化,从而反映神经元激活的区域变化。商用 fNIRS 系统使用单独的照明源和检测器。根据头围,典型的光源探测器间距在儿童中约为 1.5-3 厘米,在成人中约为 2.5-5 厘米,但建议成人间隔不超过 3.5 厘米,近年来,使用短分离通道,从光源到检测器的距离小于 1 cm,已被纳入研究中,以消除源检测器通道中头皮的血流贡献。fNIRS的局限性其一在于它的成像结果受多种噪声影响,噪声源可能包括头部运动、由于头皮上光极(源和检测器)之间的距离变化而导致的耦合随时间的变化,以及与神经元活动无关的血流变化;还会受到心率、血压波动、呼吸频率和头皮血流量等生理噪声源的影响。其二,缺乏解剖学特异性、次优的时间分辨率和个体分析的受试者内可重复性低。这些局限性限制了其在临床上的应用。

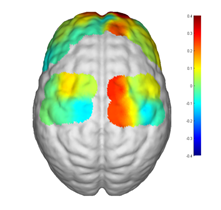
任务态下脑卒中患者fNIRS脑功能成像
c.经颅磁刺激检测(TMS)
TMS 是一种可以检测中枢运动通路的无创性检测技术,最开始用来检测量化评估脑卒中后皮层脊髓通路损伤程度以协助判断预后,后来TMS 被用于研究脑卒中后皮质-皮质回路的变化,以获得有关损伤后皮质重组的性质和程度的信息[26]。TMS可以测量脑卒中患者受影响的和未受影响的半球的初级运动皮层 (M1) 兴奋性和皮层内功能,并且通常将这些与在健康的年龄匹配的成年人中进行的相同测量进行比较 . 这些测量包括静息和活动运动阈值 (RMT, AMT)、运动诱发电位 (MEP) 幅度和潜伏期、中央运动传导时间 (CMCT)、M1 地形图体积、短间隔皮质内抑制 (SICI) 和皮质内促进 (ICF), 和皮质静默期 (CSP) ,半球间抑制,同侧静默期等。
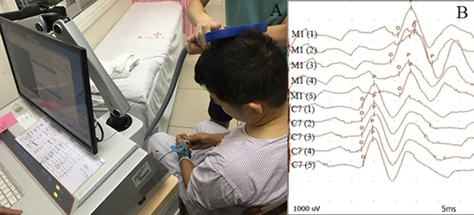
TMS检测脑卒中患者M1手功能区MEP
(4)其他评估:Neuroflexor
最近开发的一种新仪器 NeuroFlexor(Aggero MedTech AB,Solna,瑞典),可以用于量化手腕被动伸展产生的阻力的神经(痉挛)和非神经(弹性和粘性)分量。当用于测量脑卒中后的痉挛时,这个设备的测量是有效、可靠且对变化敏感的[29] 。该方法包括产生受控被动等速腕部伸展的机械装置,从而拉伸腕部和手指屈肌。力传感器测量运动过程中的阻力,并使用手的计算机生物力学模型分析力。利用以不同速度收集的数据,计算产生总被动肌肉阻力的 3 个独立分量:神经 (NC)、弹性 (EC) 和粘性 (VC) 分量。
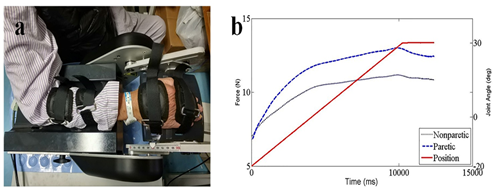
NeuroFlexor测量不同关节角度下脑卒中患者偏瘫侧与非偏瘫侧上肢肌张力变化
4.总结与展望
脑卒中在全球范围内是致死致残的主要疾病,随着人口老龄化加剧,发病率还会升高。运动功能障碍是脑卒中的最常见症状之一,对患者的日常生活影响很大,运动功能康复是康复工作者的主要目标之一,准确的运动功能评估是对促进运动功能康复至关重要,临床上最常用的运动功能评估是量表评估,但是评估具有主观性,受评估者和患者影响,客观量化的运动功能评估方法更加值得期待。评估方法根据针对的目标不同,有肢体功能评估、肌肉功能评估、中枢神经评估及肌张力评估。这些技术为脑卒中后运动功能的评估提供了客观量化的评估,我们可以对患者运动功能的康复机制有更加全面的认识,可以更好的帮助患者达到功能恢复的目的。但是目前这些评估方法也存在一些不足,尚未在临床上广泛应用,需要进一步的完善。随着科技发展,客观量化的运动功能评估方法会越来越多,应用也会越来越广泛,为脑卒中患者的康复提供更多帮助。